Pfizerning COVID uchun mRNK vaktsinasi ribonuklein kislotasini (RNK) terapevtik maqsad sifatida ishlatishga bo'lgan ishtiyoqni qaytadan uyg'otdi.Biroq, kichik molekulalar bilan RNKni nishonga olish juda qiyin.
RNK faqat to'rtta qurilish blokiga ega: adenin (A), sitozin (C), guanin (G) va DNKda joylashgan timin (T) o'rnini bosadigan urasil (U).Bu dori selektivligini deyarli engib bo'lmaydigan to'siqga aylantiradi.Aksincha, oqsillarni tashkil etuvchi 22 ta tabiiy aminokislotalar mavjud bo'lib, bu ko'pchilik oqsilga mo'ljallangan dorilarning nisbatan yaxshi selektivlikka ega ekanligini tushuntiradi.
RNKning tuzilishi va funktsiyasi
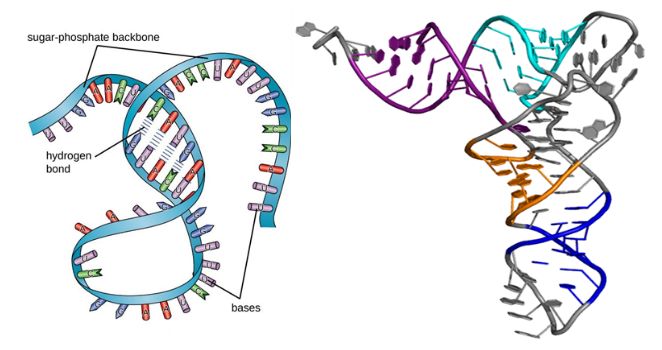
Oqsillar singari, RNK molekulalari quyidagi rasmda ko'rsatilganidek, ikkilamchi va uchinchi darajali tuzilishga ega.Ular bir zanjirli makromolekulalar bo'lishiga qaramasdan, ularning ikkilamchi tuzilishi asoslar juftligi bo'rtiqlar, halqalar va spirallarga sabab bo'lganda shakllanadi.Keyinchalik, uch o'lchovli katlama RNKning uchinchi darajali tuzilishiga olib keladi, bu uning barqarorligi va funktsiyasi uchun zarurdir.
1-rasm. RNKning tuzilishi
RNKning uch turi mavjud:
- Messenger RNK (mRNK)DNKdan genetik ma'lumotni transkripsiya qiladi va ribosomaga asosiy ketma-ketlik sifatida o'tkaziladi;l
- Ribosomal RNK (rRNK)sitoplazmaga eksport qilinadigan va mRNKdagi ma'lumotlarni oqsillarga aylantirishga yordam beradigan ribosomalar deb ataladigan oqsil sintezlovchi organellalarning bir qismidir;
- Transfer RNK (tRNK)mRNK va oqsilni tashkil etuvchi aminokislotalar zanjiri o'rtasidagi aloqadir.
RNKni terapevtik maqsad sifatida nishonlash juda jozibali.Bizning genomimizning atigi 1,5 foizi oxir-oqibat oqsilga, 70-90 foizi esa RNKga transkripsiyalanganligi aniqlandi.RNK molekulalari barcha tirik organizmlar uchun eng muhim hisoblanadi.Frensis Krikning "markaziy dogma" ga ko'ra, RNKning eng muhim roli genetik ma'lumotni DNKdan oqsillarga aylantirishdir.Bundan tashqari, RNK molekulalari boshqa funktsiyalarga ega, jumladan:
- Oqsil sintezida adapter molekulalar vazifasini bajaradi;l
- DNK va ribosoma o'rtasida xabarchi bo'lib xizmat qiladi;l
- Ular barcha tirik hujayralardagi genetik ma'lumotlarning tashuvchilari;l
- Yangi oqsillarni sintez qilish uchun zarur bo'lgan to'g'ri aminokislotalarning ribosomal tanlovini rag'batlantirishin vivo.
Antibiotiklar
1940-yillarning boshida kashf qilinganiga qaramay, ko'plab antibiotiklarning ta'sir qilish mexanizmi 1980-yillarning oxirigacha aniqlanmagan.Aniqlanishicha, antibiotiklarning katta qismi bakterial ribosomalarga bog‘lanib, ularning tegishli oqsillarni hosil qilishiga yo‘l qo‘ymaydi va shu bilan bakteriyalarni o‘ldiradi.
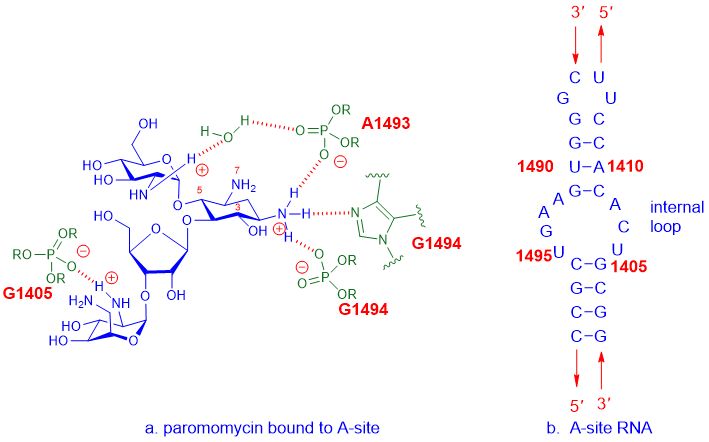
Masalan, aminoglikozidli antibiotiklar 30S ribosoma subunitiga kiruvchi 16S rRNKning A-joyiga bog‘lanadi, so‘ngra oqsil sinteziga aralashib, bakteriya o‘sishiga to‘sqinlik qiladi va natijada hujayra o‘limiga olib keladi.A-sayt tRNK qabul qiluvchi sayt sifatida ham tanilgan aminoatsil uchastkasiga ishora qiladi.kabi aminoglikozid preparatlari o'rtasidagi batafsil o'zaro ta'sirparomomisin, va A-saytiE. coliRNK quyida ko'rsatilgan.
Shakl 2. Paromomisin va A-sayt o'rtasidagi o'zaro ta'sirE. coliRNK
Afsuski, ko'plab A-sayt inhibitörleri, shu jumladan aminoglikozid preparatlari, nefrotoksiklik, dozaga bog'liq va o'ziga xos qaytarilmas ototoksiklik kabi xavfsizlik muammolariga ega.Ushbu zaharlanishlar RNKning kichik molekulalarini tanib olish uchun aminoglikozid preparatlarida selektivlikning yo'qligi natijasidir.
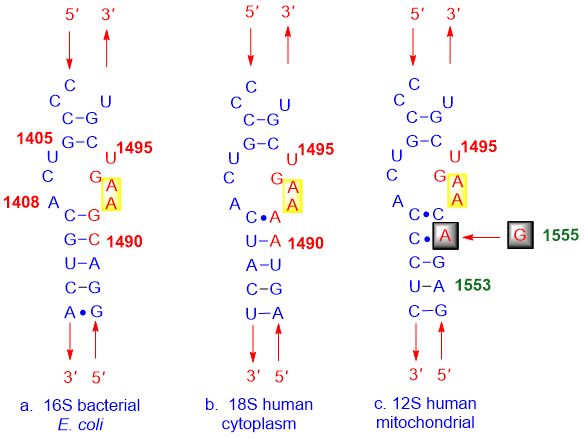
Quyidagi rasmda ko'rsatilganidek: (a) bakteriyalarning tuzilishi, (b) inson hujayra membranasi va (c) odamning mitoxondrial A-saytlari juda o'xshash bo'lib, A-sayt ingibitorlarini ularning barchasi bilan bog'laydi.
Shakl 3. Tanlanmagan A-sayt inhibitori bog'lanishi
Tetratsiklin antibiotiklari ham rRNKning A-sahifasini inhibe qiladi.Ular Mg bilan komplekslangan 30S subunitidagi spiral mintaqaga (H34) teskari bog'lanish orqali bakterial oqsil sintezini tanlab inhibe qiladi.2+.
Boshqa tomondan, makrolid antibiotiklari yangi paydo bo'lgan peptidlar (NPET) uchun bakterial ribosoma tunnelining chiqish joyi (E-sayt) yaqinida bog'lanadi va uni qisman bloklaydi va shu bilan bakterial oqsil sintezini inhibe qiladi.Nihoyat, oksazolidinon kabi antibiotiklarlinezolid(Zyvox) 23S rRNK nukleotidlari bilan o'ralgan bakterial 50S ribosoma bo'linmasidagi chuqur yoriq bilan bog'lanadi.
Antisens oligonükleotidlar (ASO)
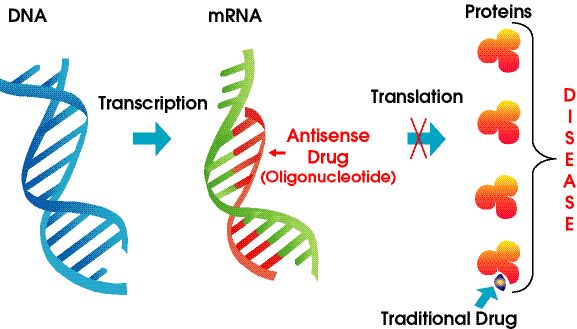
Antisens preparatlari kimyoviy modifikatsiyalangan nuklein kislota polimerlari bo'lib, ular RNKni nishonga oladi.Ular maqsadli mRNK bilan bog'lanish uchun Uotson-Krik asoslari juftligiga tayanadi, natijada gen sustlashuvi, sterik blokada yoki splicing o'zgarishi sodir bo'ladi.ASO lar hujayra yadrosidagi pre-RNKlar va sitoplazmadagi etuk mRNKlar bilan o'zaro ta'sir qilishi mumkin.Ular ekzonlar, intronlar va tarjima qilinmagan hududlarni (UTR) nishonga olishlari mumkin.Bugungi kunga qadar o'ndan ortiq ASO dori-darmonlari FDA tomonidan tasdiqlangan.
Shakl 4. Antisens texnologiyasi
RNKga qaratilgan kichik molekulali dorilar
2015-yilda Novartis ular U1-pre-mRNK assotsiatsiyasini kuchaytiruvchi va SMA sichqonlarini qutqaruvchi Branaplam deb nomlangan SMN2 splicing regulyatorini kashf qilganliklarini xabar qildi.
Boshqa tomondan, PTC/Roche's Risdiplam (Evrysdi) FDA tomonidan 2020 yilda SMA ni davolash uchun tasdiqlangan.Branaplam singari, Risdiplam ham funktsional SMN oqsillarini ishlab chiqarish uchun tegishli SMN2 genlarini birlashtirishni tartibga solish orqali ishlaydi.
RNK degradatorlari
RBM RNK-bog'lovchi motif oqsilini anglatadi.Asosan, indol sulfanilamid molekulyar yopishtiruvchidir.U RBM39 ni CRL4-DCAF15 E3 ubiquitin ligazaga tanlab oladi, bu RBM39 poliubiquitinatsiyasini va oqsillarni parchalanishini rag'batlantiradi.RBM39 ning irsiy kamayishi yoki sulfanilamid vositachiligida degradatsiyasi genom bo'ylab sezilarli anormalliklarni keltirib chiqaradi va natijada hujayra o'limiga olib keladi.
RNK-PROTAClar RNK-bog'lovchi oqsillarni (RBP) parchalash uchun ishlab chiqilgan.PROTAC E3 ligaza ligandini RNK va RBP bilan bog'laydigan RNK ligandiga ulash uchun bog'lovchidan foydalanadi.RBP o'ziga xos oligonükleotid ketma-ketliklari bilan bog'lanishi mumkin bo'lgan strukturaviy domenlarni o'z ichiga olganligi sababli, RNK-PROTAC oligonükleotidlar ketma-ketligini qiziqtiradigan protein (POI) uchun ligand sifatida ishlatadi.Yakuniy natija - RBPlarning degradatsiyasi.
Yaqinda Skripps Okeanografiya Instituti professori Metyu Disney RNKni ixtiro qildi.ribonukleazalarni maqsad qilgan kimeralar (RiboTACs).RiboTAC - bu RNase L ligand va RNK ligandni bog'lovchi bilan bog'laydigan geterofunktsional molekula.U endogen RNase L ni maxsus RNK maqsadlariga jalb qilishi va keyin hujayrali nuklein kislotaning parchalanish mexanizmi (RNase L) yordamida RNKni muvaffaqiyatli yo'q qilishi mumkin.
Tadqiqotchilar kichik molekulalar va RNK maqsadlari o'rtasidagi o'zaro ta'sir haqida ko'proq ma'lumotga ega bo'lgach, kelajakda bu usuldan foydalanadigan ko'proq dorilar paydo bo'ladi.
Yuborilgan vaqt: 2023-yil 2-avgust